Као што Профаге фазна ДНА умерених бактериофага назива се када је присутна у ћелији бактеријског домаћина. Бактериофаге је открио Фелик Хуберт д'Хререлле 1917. године. То су вируси који су се прилагодили специфичним бактеријама. У даљем току истраживања направљена је разлика између литског фага са високом вируленцијом и умереног фага са тихим профагом и лизогеног циклуса.
Шта су профаги?
Профаге умјереног бактериофага могу бити присутне као плазмид у ћелији домаћина или бити интегриране у бактеријску ДНК. За то, умерени фаг мора да усвоји лизогени циклус када се ињекује ДНК фага. Разликује се од литског циклуса и лизогеног циклуса. Док литски циклус узрокује брзу репликацију и накнадну лизу ћелије домаћина након убризгавања генетског материјала, у лизогени циклус се репресорски гени фага убризгавају у ћелију домаћина да би се сузбио литски циклус, тј. Брзо растварање ћелије.
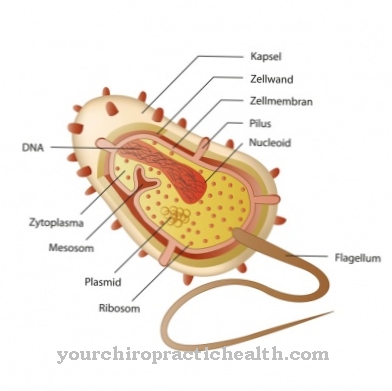
Умерени фаг може да се пребаци између литског и лизогеног циклуса у зависности од преовлађујућих животних услова. Литички циклус се односи на конвенционални начин на који фаги гени дјелују унутар ћелије домаћина. Брза репликација унутар ћелије домаћина догађа се након убризгавања вирусне ДНК. Након што се капсид и протеински репни влакни реплицирају поред вирусне ДНК и бројне нове вирусне честице су сакупљене из појединих делова, ћелијска стијенка ћелије домаћина се разграђује лизоцимом. Када се ћелијски зид растопи, нови фагови се ослобађају и њихова ДНК се сада може убризгати у друге бактеријске ћелије. Овај процес је завршен за око сат времена.
Због великог броја нових вирусних честица, овај приступ се назива "вирулентни облик". Пошто је ћелијска стијенка домаћина уништена лизоцимом, користи се термин "литски циклус". У случају умереног фага, брза репликација и каснија лиза ћелије домаћина не морају нужно да ступе на снагу. У зависности од постојећих фактора животне средине, умерени фаг може прелазити из циклуса лизе у лизогени циклус. Литички циклус се може сузбити убризгавањем репресивних гена и лизогени циклус може започети у недоглед.
У лизогеном циклусу генетски материјал фага се убацује у генетски материјал клице и овде може да опстане неодређено време. Ињектирани генетски материјал назива се "миран" и дефинисан је као "профај". Профаг може лежати као плазмид у цитоплазми ћелије домаћина или бити интегрисан у генетски материјал бактерије.
Интеграција вирусног генетског материјала захтева висок степен специјализације. Геном умјерених фагова може бити причвршћен само на одређене положаје у бактеријској ДНК. Супротно томе, генетски материјал појединих сојева умереног фага увек се може идентификовати на истим локацијама бактеријског генома.
Успешна адаптација чини профаге корисницама поделе бактерија. Када ћелија домаћин дели митозу, вирусни генетски материјал се преноси. Даљи пренос на друге бактерије може се одвијати коњугацијом. Профаги се, дакле, могу ширити различитим путевима преношења преко целих сојева бактерија. Због утицаја околине као што су УВ светлост или одређене хемикалије, профаг се може вратити у литски циклус и стремити агресивној репликацији.
Профаг такође користи поступке транскрипције ћелије домаћина: убризгани репресивни гени фага препознају се као оштећења ДНК од стране одређених ензима бактерије и разграђују их. Разградња репресивних гена је самоуништавајућа у ћелији домаћину. Литички циклус се више не може сузбити и профаг се мења из лизогеног стања у агресивно размножавање, што се завршава накнадним растварањем бактеријске ћелијске стијенке.
Појава, дистрибуција и својства
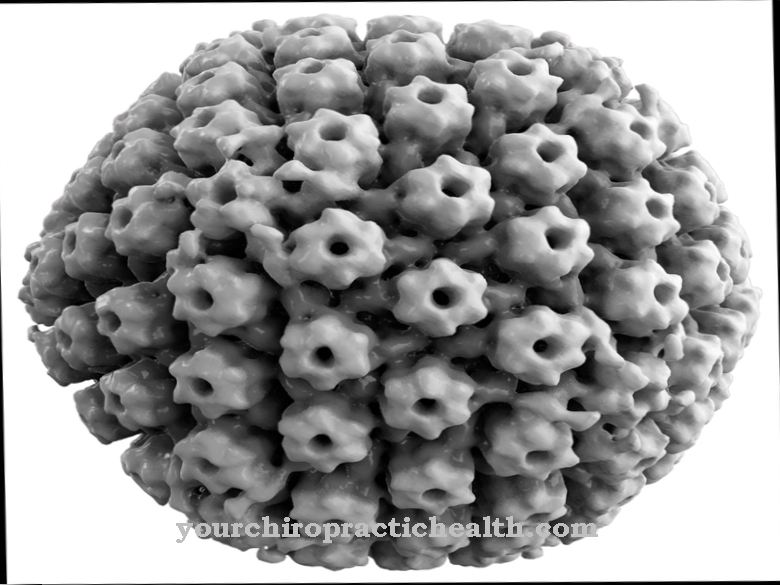
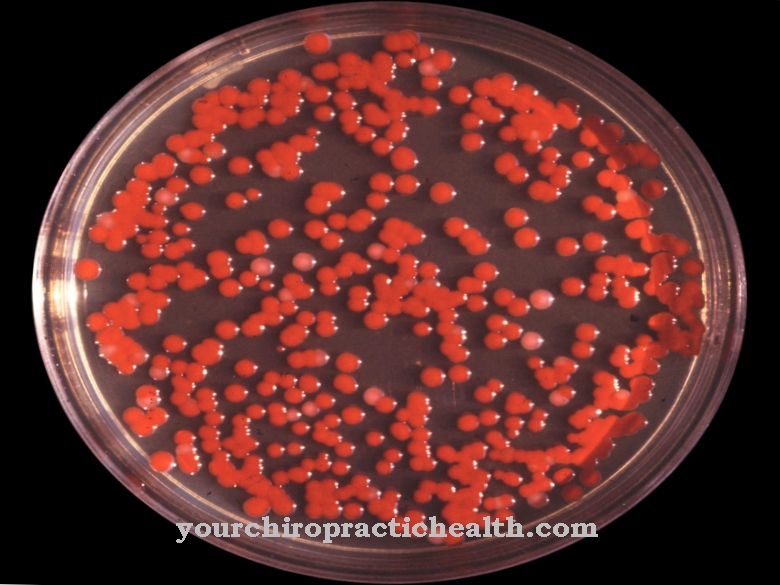
Фаги су високо специјализовани вируси који су се прилагодили појединим сојевима бактерија. Тако не може сваки бактериофаг приступити свакој бактерији. Размножавање без специфичне ћелије домаћина није могуће за бактериофаг. Висок ниво специјализације значи да се бактериофаги могу наћи на истом терену као и ћелије домаћини.
Исто је у још већој мери и за профаје. Пошто профаги нису уобичајени вируси и представљају се само као вирусни наследни материјал у организму домаћина, они се не могу наћи изван одређених ћелија због саме дефиниције.
Поред тога, мора се споменути да сами бактериофаги у морској води имају број (10 до снаге 30) и самим тим више фага него живих бића има на целој планети. Супротно томе, постоји врло мали број од деветнаест званично истражених бактериофага, што отежава давање прецизне изјаве о тој појави.
Значење и функција
Фаго терапија је развијена 1920-их година и успешно се користи у Источној Европи за борбу против разних заразних болести до данас. Предности фаго терапије су очигледне: бактериофаги штете само појединим сојевима бактерија, док антибиотици имају опште штетни утицај на бактерије у телу.
Откриће пеницилина четрдесетих година КСКС века довело је до масовне употребе антибиотика на Западу и, као резултат, окончало фаг истраживање. Накнадна накупина бројних резистенција на антибиотике покренула је повећано интересовање за бактериофаге у деведесетима.
Фаго терапија се фокусира на бактериофаге са агресивном вируленцијом и искључиво личким циклусом, док умерени бактериофаги и профаги до сада имају само подређену улогу.
Болести и тегобе
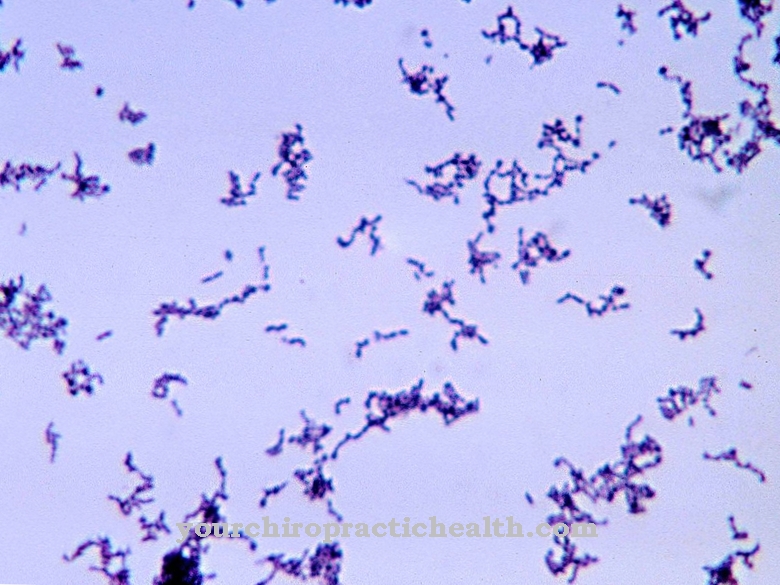
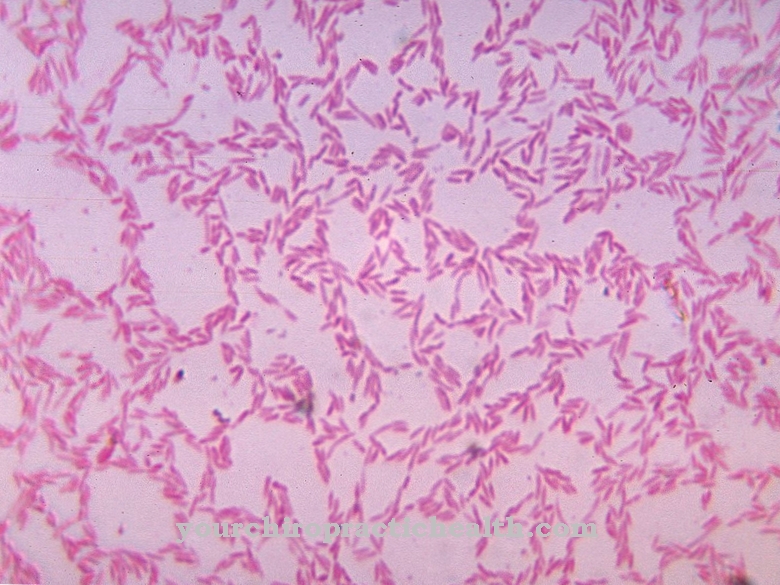
Неки патогени могу изградити своју вируленцију само кроз симбиозу са профазима. Цлостридиум ботулинум може произвести грозан ботулин токсин само уз помоћ интегрисане ДНК фага. Стрептоцоццус пиогенес може изазвати шкрлетну температуру само у комбинацији са ДНК профага.
Вибрио колере производе колеру само кроз посебне профаге. Ово такође показује важност фагова за људску медицину. Цијели бактеријски сојеви могли би изгубити свој патогени потенцијал ако се одговорни профаги могу посебно искључити.


.jpg)


.jpg)






.jpg)