Тхе Водикова веза је интеракција између молекула која подсећа на Ван дер Ваалсове интеракције и дешава се у људском телу. Веза има улогу посебно у вези са пептидним везама и ланцима аминокиселина у протеинима. Организам није одржив без способности везивања водоника јер му недостају виталне аминокиселине.
Шта је водоничка веза?

Називају се водоничне везе Водоничне везе или Х мостови скраћено. То је хемијски ефекат који се односи на атрактивну интеракцију ковалентно повезаних атома водоника са слободним електронским паровима атома који групира атом. Интеракција се заснива на поларитету и, прецизније описано, састоји се између позитивно поларизованих атома водоника у амино или хидроксилној групи и усамљених парова електрона у другим функционалним групама.
До интеракције долази само под одређеним околностима. Један од услова је електронегативно својство парова слободних електрона. Ово својство мора бити јаче од електронегативног својства водоника да би се створила снажна веза. Атом водоника се тако може везати поларно. Електронегативно слободни атоми могу бити, на пример, азот, кисеоник и флуор.
Водоничне везе су секундарне валентне везе, чија је снага обично далеко испод снаге ковалентних или јонских веза. Молекули у водоничним везама имају релативно високу тачку топљења и слично високу тачку кључања у односу на своју моларну масу. Везе су од медицинског значаја пре свега у односу на пептиде и нуклеинске киселине у организму.
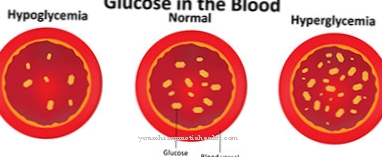
Водикове везе су интермолекуларне силе. Без њиховог постојања, вода не би постојала у разним агрегатним стањима, већ би била гасовита.
Функција и задатак
Водонска веза има само слабу интеракцију и јавља се између две честице или унутар молекула. У том контексту облик везе игра улогу, на пример, за формирање терцијарних структура у протеинима. У биохемији, структура протеина значи различите структурне нивое протеина или пептида. Структуре ових природних супстанци хијерархијски су подељене на примарну структуру, секундарну структуру, терцијарну структуру и квартарну структуру.
Низ амино киселина је примарна структура. Кад год се протеин помиње у односу на његов просторни распоред, често се помиње и конформација протеина и феномен промене конформације. У овом контексту, промена конформације одговара промени просторне структуре. Распоред протеина заснован је на пептидној вези. Ова врста везе увек повезује аминокиселине на исти начин.
У ћелијама пептидне везе посредују рибосоми. Свака пептидна веза одговара везивању карбоксилних група једне аминокиселине и амино група друге аминокиселине, која је повезана са елиминацијом воде. Овај поступак је такође познат и као хидролиза.
У свакој пептидној вези, једна веза повезује Ц = О групу са НХ групом. Атом азота има тачно један усамљени пар електрона. Због велике електронегативности кисеоника, овај слободни пар је под утицајем извлачења електрона од О2 атома. На тај начин, кисеоник делимично повлачи усамљени пар електрона у везу између атома азота и атома угљеника, а пептидна веза поприма карактер парцијалне двоструке везе. Карактер двоструке везе елиминише слободну ротацију НХ и Ц = О група.
Атоми кисеоника и атоми водоника пептидних веза су релевантни за стварање структуре свих пептида и протеина без изузетка. На овај начин се две аминокиселине могу везати једна за другу. Након такве везаности, све пептидне везе два ланца аминокиселина су директно насупрот једна другој. Атоми водоника у пептидној вези су релативно позитивно поларизовани у поређењу са атомима кисеоника у директно супротним пептидним везама. На овај начин водоничне везе формирају и повезују два ланца аминокиселина међусобно.
Све аминокиселине у људском телу су органска једињења која се састоје од најмање једне карбокси групе и једне амино групе. Аминокиселине су битна структурна компонента људског живота. Поред α-аминокиселина протеина, познато је више од 400 непротеиногених аминокиселина са биолошким функцијама које не могу настати без везивања водоника. Силе као што је водоничка веза стабилизују терцијарну структуру аминокиселина.
Овде можете пронаћи лекове
Лекови за слабост мишићаБолести и тегобе
Ако постоји поремећај у формирању функционалних протеинско-енергетских просторних структура, обично се говори о поремећајима савијања протеина. Једно такво стање је Хунтингтон-ова болест. Овај генетски поремећај је наслеђен као аутозомно доминантно својство и настаје због генетске мутације у хромозому 4. Мутација доводи до нестабилности генског производа. Болест је неуролошка болест која је превасходно повезана са нехотичном хиперкинезијом дисталних екстремитета и лица. Перзистентна хиперкинеза доводи до крутости захваћених мишића. Поред тога, пацијенти са болешћу пате од повећане потрошње енергије.
Патолошки симптоми у вези са водоничним везама или општом структуром протеина такође су присутни код прионских болести као што су болест луде краве. Према најпопуларнијој хипотези, БСЕ изазива погрешно савијање протеина. Ови погрешно савијани протеини се не могу разградити физиолошким процесима и зато се накупљају у ткиву, посебно у централном нервном систему. Резултат је дегенерација нервних ћелија.
О малформацијама протеинске структуре такође се расправља у узрочној повезаности Алзхеимерове болести. Споменуте болести не утичу директно на водоничну везу, већ се односе на просторну структуру протеина, чему водоник веза даје значајан допринос.
Организам са апсолутном неспособношћу везања на водоник није одржив. Мутација која узрокује то би довела до побачаја у раној трудноћи.







.jpg)

.jpg)





.jpg)